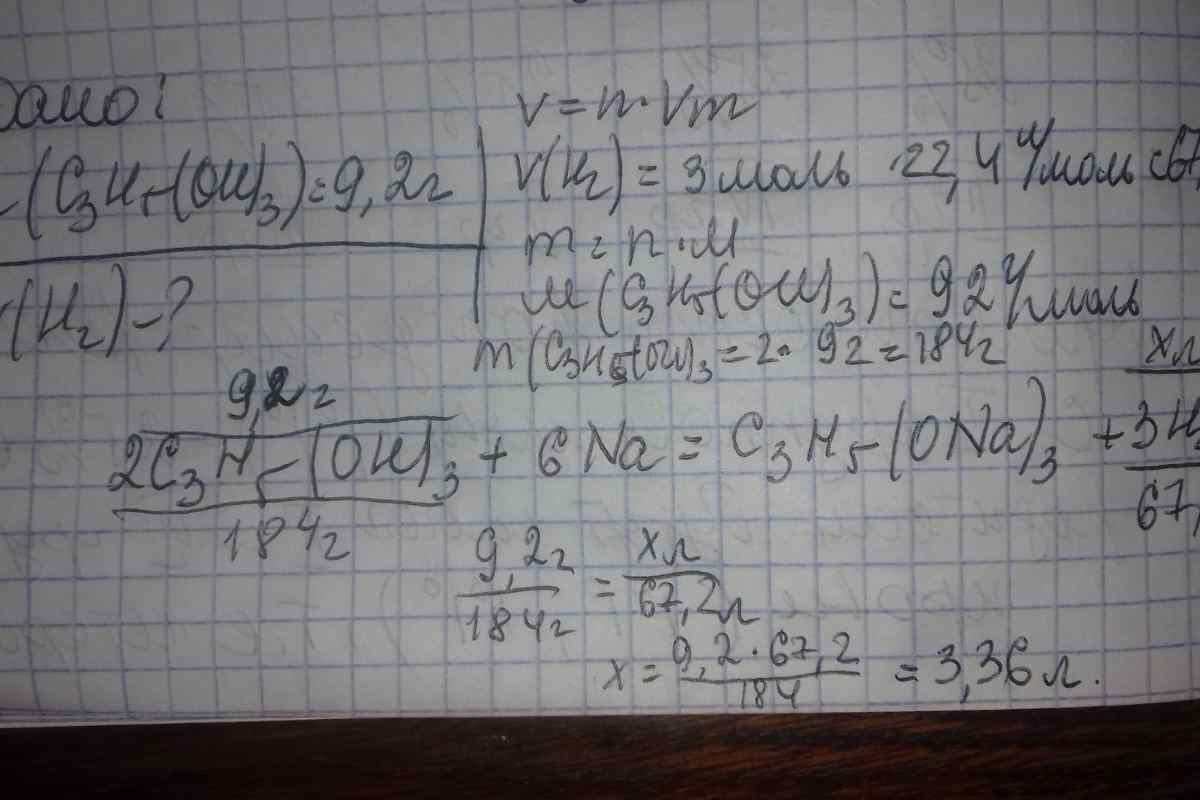У навчальному курсі хімії часто зустрічаються завдання, в яких потрібно обчислити обсяг газу, що виділився в результаті хімічної реакції. Майже всі завдання такого типу можна вирішити за наступним алгоритмом.
Вам знадобиться
- - таблиця Менделєєва;
- - ручка;
- - папір для записів.
Інструкція
1. Наприклад, вам потрібно знайти обсяг виділеного водню в результаті реакції ортофосфорної кислоти і карбонату натрію. Найголовніше для рішення - правильно скласти рівняння реакцій. Якщо ви сумніваєтеся, як реагують дані у вашому завданні речовини, подивіться в довідковій літературі властивості хімічних речовин, що беруть участь у реакції.
2. Розставте коефіцієнти рівняння, щоб кількість атомів елементів у лівій та правій частині рівняння збігалася. Тепер ви бачите, в якому співвідношенні реагують речовини. За відомою кількістю будь-якого з них ви можете визначити кількість молей газу, що виділився. Наприклад, якщо в реакцію вступило 4 молі ортофосфорної кислоти, вийде 6 молей вуглекислого газу.
3. Знаючи кількість молей газу, знайдіть його обсяг. За законом Авогадро 1 моль будь-якого газу в нормальних умовах займає 22,4 літра обсягу. Обсяг 6 молей газу дорівнюватиме: 6 * 22,4 = 134,4 літра.
4. Якщо в умові не дано кількість реагенту або продукту реакції, знайдіть з його інших даних. При відомій масі однієї з речовин ви вирахуєте його кількість молей за формулою: v = m/M, де v - кількість речовини, моль; m - маса речовини, г; M - молярна маса речовини, г/моль. Молярну масу ви отримаєте, склавши атомні ваги елементів, що складають речовину, з таблиці Менделєєва. Наприклад, молярна маса H3PO4: М = 3 * 1 + 31 + 16 * 4 = 98 р/моль.
5. Масу або кількість неважко розрахувати з концентрації речовини, якщо відомий обсяг розчину. З молярності визначте кількість молей розчиненої речовини за рівнянням: v = V * Cм, де V - об "єм розчину, л; См - молярна концентрація, моль/л. Нормальність розчину пов 'язана з молярністю виразом: Сн = z * Cм, г моль-екв/л, де z - еквівалент реагенту, кількість протонів водню, яку він може прийняти або віддати. Наприклад, еквівалент H3PO4 - 3.
6. Також масу розчиненої речовини ви можете знайти з титру розчину: m = T * V, де Т - титр розчину, г/л; V - обсяг розчину. Або з щільності: m = p * V, де р - щільність розчину, г/мл.